Introductie¶
Volgens de ideale gaswet wordt het volume van een (ideaal) gas gegeven door:
waarin
het aantal mol gas,
de ideale gasconstante,
de absolute temperatuur,
de druk.
In dit practicum veranderen we de temperatuur en meten we de verandering van het volume van het gas. De proef is met name kwalitatief van aard en laat zien hoe lastig het is een extensieve grootheid als volume te meten.
Methode en materialen¶
Ontwerp¶
Om het volume van een hoeveelheid gas bij constante druk te meten is niet zo eenvoudig. Je kunt het gas vrij eenvoudig in een ballon stoppen en dan schatten hoe de diameter van de ballon verandert als functie van de temperatuur, maar dat geeft een relatief grote fout (waarom?). We maken daarom gebruik van de wet van Archimedes.
Materialen¶
eenvoudige feestballon
bekerglas
tweede bekerglas om mee bij te vullen
thermometer
verhittingsplaat
deksel met vulcilinder met maatstrepen (met iets kleinere diameter dan interne diameter maatbeker)
(per 5 groepjes) een maatcilinder
Procedure¶
Blaas de ballon op, maar niet verder dan in diameter. Deze moet makkelijk in de maatbeker passen.
Knoop de ballon goed dicht zodat er geen lucht kan ontsnappen.
Dompel de ballon onder in de maatbeker met water met behulp van het deksel.
Pas het waterniveau aan zodat de meniscus (de bovenkant van het water) bij een van de onderste maatstrepen van de vulcilinder van het deksel zit.
Let op dat er luchtbellen kunnen plakken aan de ballon wat leidt tot een systematische fout. Verifieer dat je zo min mogelijk systematische fouten maakt en meet op welke maatstreep de meniscus zich bevindt.
Verhoog stapsgewijst de temperatuur van het water (en dus de ballon). Let op dat je de temperatuur maximaal een graad of 20 kan verhogen, want als je voorbij de vulcilinder komt met de meniscus, dan kan je de volumeverandering niet meer nauwkeurig bepalen.
Laat het geheel na elke temperatuurtoename een minuut ‘rusten’ om zo de tijd te geven om in thermisch evenwicht te komen.
Meet na elke temperatuurtoename de temperatuur en de positie van de meniscus.
Het verschiloppervlak tussen de binnendiameter van de maatbeker en de buitendiameter van de vulcilinder is . Je kunt die handmatig kalibreren met behulp van de kleine maatcilinder die in het lokaal aanwezig is. De maatstreepjes die op de vulcilinder zijn gekerfd zitten op een onderlinge afstand van .
Als je kritisch nadenkt over deze grafiek en de extrapolatie, dan kun je bezwaar maken tegen de precisie van deze proef. Het water in de maatbeker zet ook uit onder de verhoging van de temperatuur en geeft een systematische fout. Daar kun je een correctie voor uitvoeren. Voer die correctie uit als je nog genoeg tijd hebt:
Resultaten¶
import numpy as np
import matplotlib.pyplot as plt
totaal_temps = [19.3, 21.2, 29.2, 31.1, 33.2, 36.1] # graden
totaal_hoogtes = [0.9, 1.0, 1.1, 1.25, 1.3, 1.4] # cm : afstand van onderste streepje tot huidig streepje
water_temps = [19.3, 22.2, 25.9, 28.3, 36.5, 37.7] # graden
water_hoogtes = [0.75, 0.8, 0.8, 0.85, 0.9, 0.95 ] # cm
# startvolume = 325 ml
# volume meniscus = 320 ml
diam_beker = 7.66 # cm
diam_deksel = 6.77 # cm
opp_water = 1/4 * np.pi * (diam_beker**2 - diam_deksel**2) #cm2
totaal_volumes = (np.asarray(totaal_hoogtes) - totaal_hoogtes[0]) * opp_water
water_volumes = (np.asarray(water_hoogtes) - water_hoogtes[0]) * opp_water
temps_abs = np.asarray(totaal_temps) + 273
totaal_coef = np.polyfit(temps_abs, totaal_volumes, 1)
totaal_func = np.poly1d(totaal_coef)
water_coef = np.polyfit(temps_abs, water_volumes, 1)
water_func = np.poly1d(water_coef)
plt.plot(temps_abs, totaal_volumes, 'ob')
plt.plot(temps_abs, totaal_func(temps_abs), '--r')
plt.xlabel('Temperatuur [K]')
plt.ylabel('Volume Verschil [cm$^3$]')
plt.title('Met ballon')
plt.show()
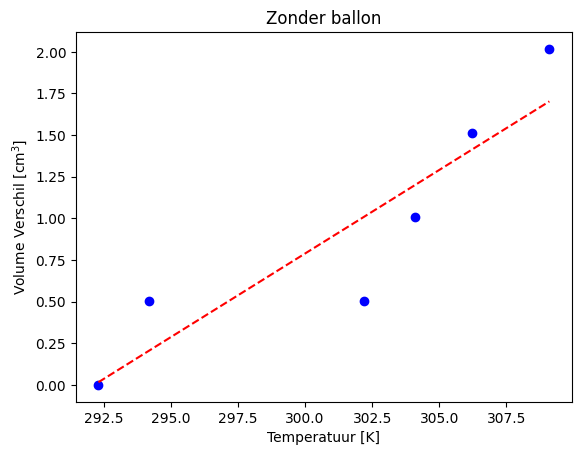
plt.plot(temps_abs, water_volumes, 'ob')
plt.plot(temps_abs, water_func(temps_abs), '--r')
plt.xlabel('Temperatuur [K]')
plt.ylabel('Volume Verschil [cm$^3$]')
plt.title('Zonder ballon')
plt.show()
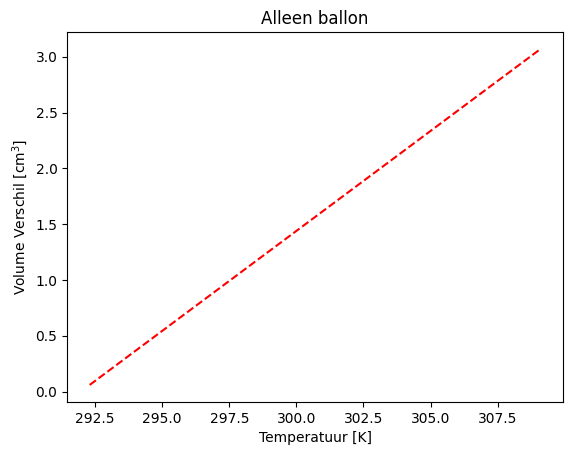
ballon_coef = np.polyfit(temps_abs, totaal_volumes, 1) - np.polyfit(temps_abs, water_volumes, 1)
ballon_func = np.poly1d(ballon_coef)
plt.plot(temps_abs, ballon_func(temps_abs), '--r')
plt.xlabel('Temperatuur [K]')
plt.ylabel('Volume Verschil [cm$^3$]')
plt.title('Alleen ballon')
plt.show()
print(totaal_func(0))
print(ballon_func(0))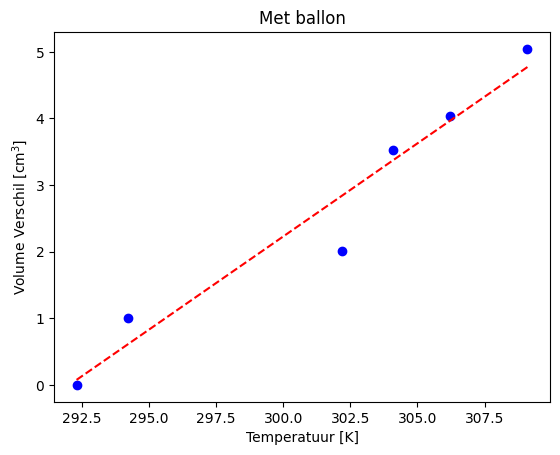
-81.63070661933193
-52.314000553213425
Discussie en conclusie¶
#Tijdens dit experiment is er vanuit gegaan van de ideale gas wet om het veranderende valume van een ballon op verschillende temperaturen
#te berekenen. Ook, om dit te versimpelen, is er aangenomen dat er een constante druk plaats neemt. Dit vervormt de ideale gas wet tot een wet
#waar alleen de volume en temperatuur niet constant zijn, en dus alleen de volume en temperatuur van belang zijn bij het meten van een verschil.
#Dit geeft rond de gemeten waarden een realistisch verschil, maar als het resulterend linear verband verder doorgerekend wordt, naar bijvoorbeeld
#het start volume bij een absolute tempteratuur van 0 K, zie je dat het af begint te wijken van de werkelijkheid. Dit is omdat de druk op de
#ballon op zulke temperaturen al snel niet constant is. Als vervolg onderzoek is het dan een start om de druk op een manier mee te rekenen.
#Ook is het mogelijk een andere methode te vinden. In elke geval leverd dit onderzoek valide resultaten rond het gemeten punt, maar wordt het
#onrealistisch rond verder verschillende temperaturen.